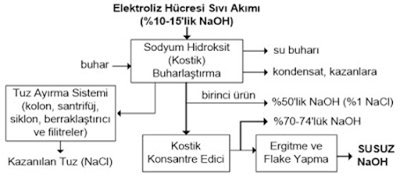
klor alkali fabrikası
Klor, 1774 yılında Alman kimyacı Scheele tarafından keşfedildi ve 1810’da İngiliz fen bilimci Davy tarafından elementel halde elde edildi. Kostik sodanın (sodyum hidroksit) kullanımı 1853 yılında başladı ve 1892’ye kadar sönmüş kireçten ve soda külünden (sodyum karbonat) üretildi. Bu tarihten sonra elektroliz yönteminin keşfedilmesiyle salamura (tuzlu su) elektrolizlenerek klor ve kostik birarada üretilmeye başlandı. 1960’lı yıllarda elektroliz işlemi bu iki önemli bileşiğin başlıca üretim prosesi oldu.
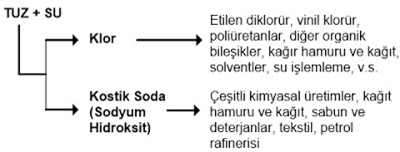
klor alkali fabrikası (Klor alkali endüstrisinin) hammaddesi sodyum klorür ve kireç taşıdır (kalsiyum karbonat); ürünler klor, sodyum hidroksit (kostik soda), soda külü (sodyum karbonat), sodyum bikarbonat, potasyum hidroksit ve potasyum karbonattır.
Üretilen klorun büyük bir kısmı organik kimyasal maddelerin elde edilmesinde kullanılmaktadır; bunlar arasında vinil klorür, etilen diklorür, gliserin, klorlu solventler ve glikoller sayılabilir. Vinil klorür üretiminde kullanılan klor %25’in üzerindedir; bilindiği gibi vinil klorür başta polivinil klorür olmak üzere çok sayıda petrokimyasalın başlangıç veya ara maddesidir. Klor kağıt endüstrisinin de önemli bir girdisidir; yıllık klor gereksinimi %10’ugeçer. Diğer kullanım alanları arasında bazı inorganik kimyasal maddelerin üretimi, su temizleme ve hipoklorit üretimi sayılabilir.
Üretilen sodyum hidroksitin yaklaşık ~%30’u organik kimya, %20’si de inorganik kimya endüstrisinde kullanılır; kağıt endüstrisinin tüketimi %20 dolayındadır. Bunlar dışında sabun ve temizlik maddeleri üretiminde ve petrol üretiminde sondaj akışkanı ve gaz ekstraksiyonu gibi yaygın kullanım alanları vardır.
Soda külü (sodyum karbonat) cam endüstrisinin temel hammaddesidir; kumun ergime noktasını düşürmede kullanılır. Endüstriyel temizlik maddelerinin temel elemanları olan sodyum fosfat ve sodyum silikat üretiminde hammaddedir. Diğer kullanım alanları metal üretimi fabrikaları, sülfit kağıt hamuru prosesleri ve tekstil prosesleri sayılabilir. Soda külünden, fosfatlar, silikatlar ve sülfitlerin üretiminde bir ara madde olarak yararlanılır.
Klor ve sodyum hidroksit elektrolizin temel iki ürünüdür ve yaklaşık olarak aynı miktarlarda elde edilirler. Elektroliz reaksiyonunun diğer bir ürünü olan hidrojen de klor ve kostikle eşit molarda çıkar. Üretimde kullanılan elektroliz hücresi tipine bağlı olmaksızın salamura hücreye girmeden önce saflaştırılır; ancak saflaştırma derecesi hücre tipine göre değişir. Tuz, doğal tuz yataklarından veya deniz suyundan sağlanabilir ve saflaştırılır. Safsızlıklar başta kalsiyum olmak üzere magnezyum, baryum, demir, aluminyum, sülfatlar ve eser metallerdir. Safsızlıklar çökelerek, membran veya diyafram maddeleri tahrip ederek elektrolitik hücreyi olumsuz yönde etkiler; ayrıca anot ve katot üzerindeki katalitik kaplamayı zehirler. Cıva hücrelerde, örneğin vanadyum gibi metaller eser miktarlarda olsalar bile verimi düşürür, tehlikeli miktarlarda hidrojen gazı çıkmasına yolaçarlar. Safsızlıkların diğer bir olumsuz etkisi de, hücre performansını düşüren klorlu bileşiklerin meydana gelmesine sebep olmasıdır.
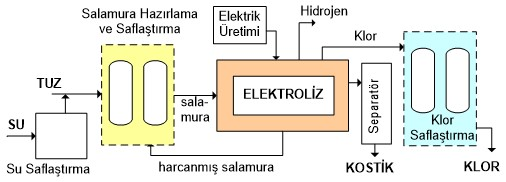
4.1.SALAMURA HAZIRLAMA
Salamura hazırlamada ilk işlem deniz tuzu veya kaya tuzunun suda çözülmesi ve karıştırmadır. Çözünebilen madde miktarı salamuranın konsantrasyonuna, karıştırma süresine ve sıcaklığa bağlıdır. Her durumda salamura-katı tuz karışımı doygunlukta dengeye gelmesi için bir süre bekletilir; yaklaşık tuz konsantrasyonu ağırlıkça %25 dolayındadır. Hazırlanan çözelti iki aşamalı saflaştırma işleminden geçirilir; bunlar:
- Na2CO3 (soda külü) ilave edilerek Ca+2, Mg+2, Fe+2, Al+3iyonlarının uzaklaştırılması
- NaOCl ilave edilerek varsa amonyağın, CaCl2 ile deSO4= iyonlarının uzaklaştırılmasıdır
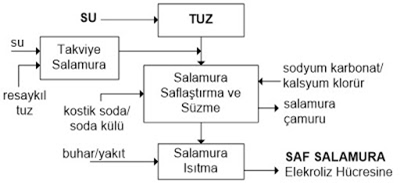
Saflaştırma bazı bileşiklerin çökelmelerini sağladığından çamurumsu bir kısım (sludge) oluşur; buna ‘salamura çamuru’ denir. Salamura çamuru yıkanarak içinde kalmış olan sodyum klorür geri kazanılır, kalan kısım atılır. Cıva hücre prosesinde salamura çamurunda eser miktarda cıva da bulunur; bu durumda çamura sodyum sülfit ilave edilerek cıva, çözünmeyen cıva sülfür bileşiğine dönüştürülür ve çamur sonra kontrollü olarak atılır.
Salamura hazırlamada ikinci aşama berraklaştırma, süzme, resaykıl salamuranın ilave edilmesi, pH ayarlama ve işlemlenmiş salamuranın tanklarda toplanmasıdır. Berraklaştırma ve süzmede kum filtreler kullanılır.
4.2. ELEKTROLİZ
Cıva ve diyafram hücre proseslerinde kullanılan salamurada en fazla 4 ppm kalsiyum ve 0.5 ppm magnezyum bulunabilir. Membran hücre prosesinde çok daha saf salamura gerekir; kalsiyum ve magnezyum toplamı 0.002ppm den az olmalıdır. Bunu sağlayabilmek için salamura iyon-değiştirici kolonlardan geçirilir.
Elektrolizde bir salamura çözeltisine iki elektrot daldırılır, elektrotlara doğru akım verildiğinde sodyum iyonları negatif elektroda (katot) doğru, klorür iyonları pozitif elektroda (anot) doğru hareket eder.
Anotta klor gazının elde edildiği (ve kostik sodadan ayrıldığı) ve katottan hidrojen gazının üretildiği üç elektrolitik proses vardır; bunlar:
- Diyafram hücreler
- Membran hücreler
- Cıva katot veya ‘amalgam’ hücreler
Bu teknolojilerin üçünde de anottan klor ve katottan hidrojen gazı çıkar. Teknolojiler arasındaki temel farklılık anolit ve katolit akımların birbirlerine karışmalarının engellenme yöntemidir. Diyafram hücrelerde bu işlev bir separatör ile, membran hücrelerde de bir iyon-değiştirici membranla sağlanır. Cıva hücreli sistemlerde katodun kendisi separatör olarak hareket eder; buradaki separatör, sodyum ve civanın birleşmesiyle oluşan amalgamdır.
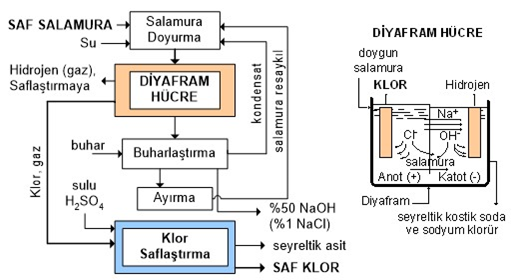
4.2.1. Diyafram Hücre Prosesi
Diyafram hücre dikdörtgen şeklinde bir kutudur; metal anot ve metal katot tabana desteklerle tutturulmuştur. Anot, rutenyum oksit veya titanyum oksit gibi oksitlerle kaplanmış titanyum levhadır. Katot, üzerinde asbest ve politetrafluo roetilen lifleri çöktürülmüş bir metaldir; bu çökelti diyafram görevi yapar. Çok sayıdaki anot-katot çifti dikey ve birbirine paralel olarak yerleştirilmiştir. Salamura sürekli olarak anot bölmesine akar, diyaframdan geçerek katoda gider. Anotta klor gazı, katotta sodyum hidroksit çözeltisi ve hidrojen oluşur. Diyafram katoda sıvının geçmesine izin verirken kabarcıklar halindeki klor gazının geçişini engeller; dolayısıyla klor ve hidrojen gazlarının karışması önlenmiş olur. Diyafram, katoda oluşan hidroksil iyonlarının geri-difüzyonunu da sınırlar. Klor ve hidrojen gazları hücrenin üst kısmından, %10-15 sodyum hidroksit içeren kalıntı salamura hücrenin dibinden alınır. Hidrojen nemi giderildikten sonra depolamaya gönderilir. Fazla saflık gerektirmeyen hallerde klor gazı önce freon veya bezeri bir soğutucuyla soğutulur, sonra dolgulu bir kolonda sülfürik asitle yıkanarak kurutulur. Kullanılmış sülfürik asit rejenere edilerek tekrar kullanılır.
Diyafram hücrelerde salamura yoluyla giren çözünmüş hava ve karbon dioksit bulunur. Bu gazlar klor saflaştırma prosesi sırasında uzaklaştırılır. Diyafram hücrenin avantajı cıva hücrelere kıyasla daha düşük voltajla çalışması ve az elektrik tüketmesidir. Ayrıca kullanılan salamura, membran ve cıva hücrelere kıyasla daha az saflıktadır.
| Anodik reaksiyon | Katodik reaksiyon |
| 2Cl– ® Cl2 + 2e– | 2H2O + 2e– ® 2OH– + H2 |
| Toplam iyonik reaksiyon | Toplam reaksiyon |
| 2Cl– + 2H2O ® Cl2 + H2 + 2OH– | 2NaCl + 2H2O® Cl2 +2NaOH + H2 |
| Yan reaksiyon | Yan reaksiyon |
| Cl2 + 2NaOH® NaOCl + NaCl + H2O | 3NaOCl ® NaClO3 + 2NaCl |
4.2.2. Membran Hücre Prosesi
Bir membran hücrede anot ve katot kompartımanları bir iyon değiştirici membranla birbirinden ayrılır. Membran, genellikle çift tabakalıdır; perfluoro-karboksilik asit ve perfluorosülfonik asit bazlı filmlerin sıkıştırılmasıyla hazırlanır. Membran su geçirmez, fakat iyonları seçerek geçirir özelliktedir.
Katot bir katalizörle kaplanmış paslanmaz çelik veya nikeldir (nikel-sülfür, nikel-aluminyum, nikel-nikel oksit veya platin grubu metaller). Kaplamanın amacı yüzey alanı artırmak ve hidrojen çıkış potansiyelini düşürmektir. Anot, diyafram ve cıva hücrelerde olduğu gibi rutenyum veya titanyum-titanyum oksittir.
Proseste doygun salamura çözeltisi anot bölmesine verilir; anottan klor gazı çıkarken sodyum iyonları membrandan geçerek katot kompartımanına girer. Katotta suyun hidroliziyle H2 gazı çıkarken membrandan geçerek gelen sodyum iyonları hidroksil iyonlarıyla birleşerek sodyum hidroksit (%30-33’lük) oluşur.
Membran pozitif yüklü sodyum iyonlarını anot bölmesinden katot bölmesine geçirir, ancak negatif yüklü klorür iyonlarını ve hidroksil iyonlarını bir taraftan diğer tarafa geçirmez.
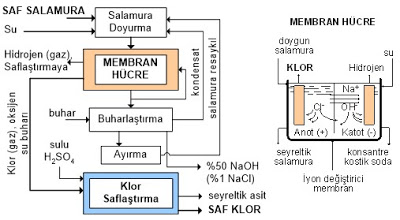
Bu nedenle elde edilen sodyum hidroksit çözeltisindeki NaCl eser miktardadır (<100 ppm). Anodu terkeden harcanmış seyreltik salamura tuzla tekrar konsantre edilerek yeniden kullanıma alınır.
Membran hücrenin dezavantajları elde edilen klor gazında uzaklaştırılması gereken oksijen ve su buharı bulunması ve kostik çözeltisinin konsantrasyonunun artırılmasıdır; bunlar ilave prosesler gerektirir.
Diğer bir olumsuzluk membranın kirlenmemesi için elektroliz hücresine verilen salamuranın çok yüksek saflıkta olması gereğidir; bu da ileri salamura saflaştırma prosesleriyle yapılır ve doğal olarak maliyeti artırır. Membran ayırıcılar pahalıdır, kolay bozulurlar ve kullanım süreleri, diyafram ve cıva separatörlerden daha kısadır.
4.2.3. Cıva Hücre Prosesi
Cıva hücreli proseste biri cıva hücresi, diğeri bozundurma hücresi olmak üzere iki hücre yeralır. Elektroliz hücresi dikdörtgen biçiminde büyük bir çelik kaptır; duvarları esnek ve yanmaya dayanıklı kauçukla kaplıdır. Dipten 3 mm kadar yüksekliğe kadar doldurulmuş olan ince bir cıva tabakası katot görevi yapar. Civanın üstünde ~%25’lik (ağ.) sodyum klorür çözeltisi (salamura) bulunur.
Anot, salamura çözelti içine daldırılmış üzerleri rutenyum oksit ve titanyum oksitle kaplanmış titanyum levhalardır; salamura içindeki yükseklikleri cıva katoda göre ayarlanır.
Elektroliz hücresinde sodyum klorürün iyonlaşmasıyla klor gazı çıkar, gaz ekstraksiyon yarıklarından geçerek klor saflaştırma ünitesine gider. Sodyum iyonları cıva tabakasında absorblanır; oluşan amalgam (sodyum ve civa karışımı) bozundurma hücresine verilir.
Bozundurma hücresi amalgamın katot, grafit levhaların da anot görevi yaptığı galvanik bir pildir; hücre iki bölümlü küçük silindirik bir çelik kolondur. Amalgam kolonun üst kısmından girer, kısmen bozunur ve alt bölüme geçer, burada bozunma işlemi tamamlanır. Hücre boyunca akan amalgam ve su, grafitle doğrudan temas halindedir, dolayısıyla amalgamın suyla parçalanarak sodyum hidroksit oluşumu, civanın geri kazanılması ve hidrojen gazı üretimi kolonun her iki bölümünde de gerçekleşir. Kazanılan cıva ilk elektroliz hücresine döndürülür. Sodyum hidroksit (~%50) olduğu gibi kullanılır, satılır veya konsantre edilerek yararlanılır. Hidrojen gazı saflaştırıldıktan sonra fabrika veya kompleks içinde kullanılır.
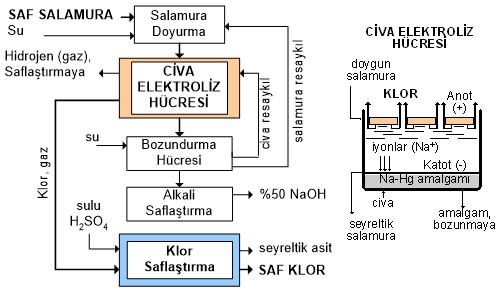
Hücreden çıkan kullanılmış salamura (NaCl %21-22 ağ.) içerdiği çözünmüş klordan arındırılıp sodyum klorürle doyurulur, saflaştırılır ve tekrar elektroliz hücresine verilir.
Cıva hücre prosesinin avantajlı tarafı proseste elde edilen sodyum hidroksitin yüksek konsantrasyonda (%50) olması ve kalıntı tuz oluşmamasıdır, ancak diyafram ve membran hücre proseslerine göre daha fazla voltaja gereksinimi olduğundan elektrik tüketimi yüksektir. Ayrıca cıva atıkları ve emisyonlarının çevre kirliliği kriterlerine uyması gereği bu prosesin kullanımını sınırlar.
| Anodik reaksiyon: | 2Cl– ® Cl2 + 2e– |
| Katodik reaksiyon: | 2Na+ + 2Hg + 2e–® 2Na (in Hg) |
| Toplam hücre: | 2Cl– + 2Na+ + 2Hg ® Cl2 + 2Na (in Hg) |
| Bozundurma: | 2Na (in Hg) + 2H2O ® H2 +2NaOH + Hg |
| Toplam proses: | 2NaCl + 2H2O ® Cl2 +2NaOH + H2 |
4.3. ÜRÜNLER
4.3.1. Klor
Elektroliz hücresinin anot kompartımanından çıkan gaz klorda nem, oksijen ve çok az hidrojen ve hava vardır.
Klor gazı önce 60oF (16oC)’ye soğutulur, içerdiği damlacıklar halindeki su taneciklerini uzaklaştırmak için demisterlerden geçirilir ve sonra kalan nemin de ayrılması için bir dizi sülfürik asit sirkülasyon kolonlarına gönderilir. Kurutulmuş klor gazı tekrar demisterlere ve oradan da sıkıştırma-soğutmaya verilerek düşük sıcaklıkta sıvılaştırılır.
Sıvılaşmadan kalan gaza ‘snift’ gaz denir; bu gaz kostik soda veya kireçle (kalsiyum hidroksit) nötralleştirilerek hipoklorit olarak satılır veya hidroklorik asir üretiminde kullanılır. Sıvı klor ‘taffy’’ denilen klorlanmış ağır bileşiklerden arındırılmak için fraksiyonlu distilasyon kolonunda distillenir. Hafif fraksiyonlar hava, karbon dioksit gibi inert gazlarla brom ve iyot gibi safsızlıklar içerir.
4.3.2. Sodyum Hidroksit
Kostik soda %50, %73 ve susuz (kuru) taneler veya yapraklar halinde pazarlanır. Cıva hücreli elektroliz prosesinde elde edilen kostik %50 ve %70 74’lüktür; dolayısıyla konsantrasyon artırmak için ilave proseslere gerek olmaz. Ancak bir miktar cıva içerdiğinden bozundurucudan çıkan kostik soğutulup aktif karbon filtreden geçirilerek cıva ppm seviyelerine düşürülür. Yine de bazı tüketiciler cıva prosesiyle üretilen kostiği kullanmak istemezler. Diğer safsızlıklar yönünden bakıldığında kostik soda cıva prosesinden elde edilir.
Diyafram ve membran elektroliz hücrelerinden çıkan sodyum hidroksit seyreltik olduğundan konsantrasyonun artırılması için buharlaştırma prosesine gerek vardır. Diyafram hücre prosesinin en büyük dezavantajı fazla miktarda tuz içermesidir. Tuzun azaltılması için tuz kolonları, santrifüjler, siklonlar, berraklaştırıcılar ve filtrelere gerek vardır; bütün bu işlemler prosesi karmaşıklaştırır, enerji tüketimini ve maliyeti artırır. Şekil-4.6 bir diyafram hücreden çıkan %10-15’lik kostik çözeltisinin konsantrasyonunun yükseltilmesi için gerekli proses akışını göstermektedir.
4.3.3. Hidrojen
Klor alkali fabrikasından çıkan hidrojen genellikle hidroklorik asit üretiminde veya buhar üretimi için yakıt olarak kullanılır. Cıva hücre prosesinden alınan hidrojen içerdiği civanın uzaklaştırılması için önce soğutulur, civanın büyük kısmı burada ayrılır, sonra eser miktardaki cıva da hidrojen gazının moleküler elekli kolondan geçirilmesiyle giderilir.
| Klor, Cl2 | Sodyum hidroksit (Kostik soda), NaOH | Hidrojen, H – H | |
| Görünüş | renksiz, gaz | Beyaz, katı | gaz |
| Molekül Ağ, g/mol. | 70,906 | 40 | 2 |
| Yoğunluk, g/cm3, 20 0C | 3.21X10 –3 | 2.1 | 0.08988×10-3 |
| Alevlenme nok. 0C | alevlenmez | ||
| Erime nok., 0C | -101 | 323 | −259.14 |
| Kaynama nok., 0C | -34.6 | 1390 | −252.87 |
| Çözünürlük, suda | 0.7 g/100 ml | çözünür | – |
Firmamız hakkında bilgi almak için buraya tıklayınız.
Instagram sayfamızı takip etmek için buraya tıklayınız.